Il termine soluzione, in chimica, viene utilizzato per indicare una miscela le cui sostanze ivi contenute si presentano in fase o liquida, solida o gassosa e le cui particelle risultano distibuite in maniera equa e uniforme nello spazio occupato, in modo tale che tutti i volumi della soluzione in oggetto abbiano la stessa composizione degli altri.
Una soluzione è composta da due elementi: il soluto (sostanza presente in quantità inferiore) e il solvente (sostanza predominante). Nelle occorrenze in cui le sostanze siano solubili fra loro in qualsiasi proporzione, queste sono denominate miscibili.
La caratteristica distintiva delle soluzioni rispetto a una dispersione generica è detta solvatazione. Questo tratto definisce la composizione del soluto, il quale risulta disperso nel solvente sul piano dei singoli ioni o molecole, ognuno dei quali viene circondato da molecole di solvente.
Nel caso in cui un il soluto sia composto da atomi di dimensioni minori di 1 nm, la miscela è detta soluzione vera, mentre si parla di soluzione falsa o dispersione colloidale nell’evetualità in cui le particelle siano di grandeza compresa tra 1 e 1000 nm.
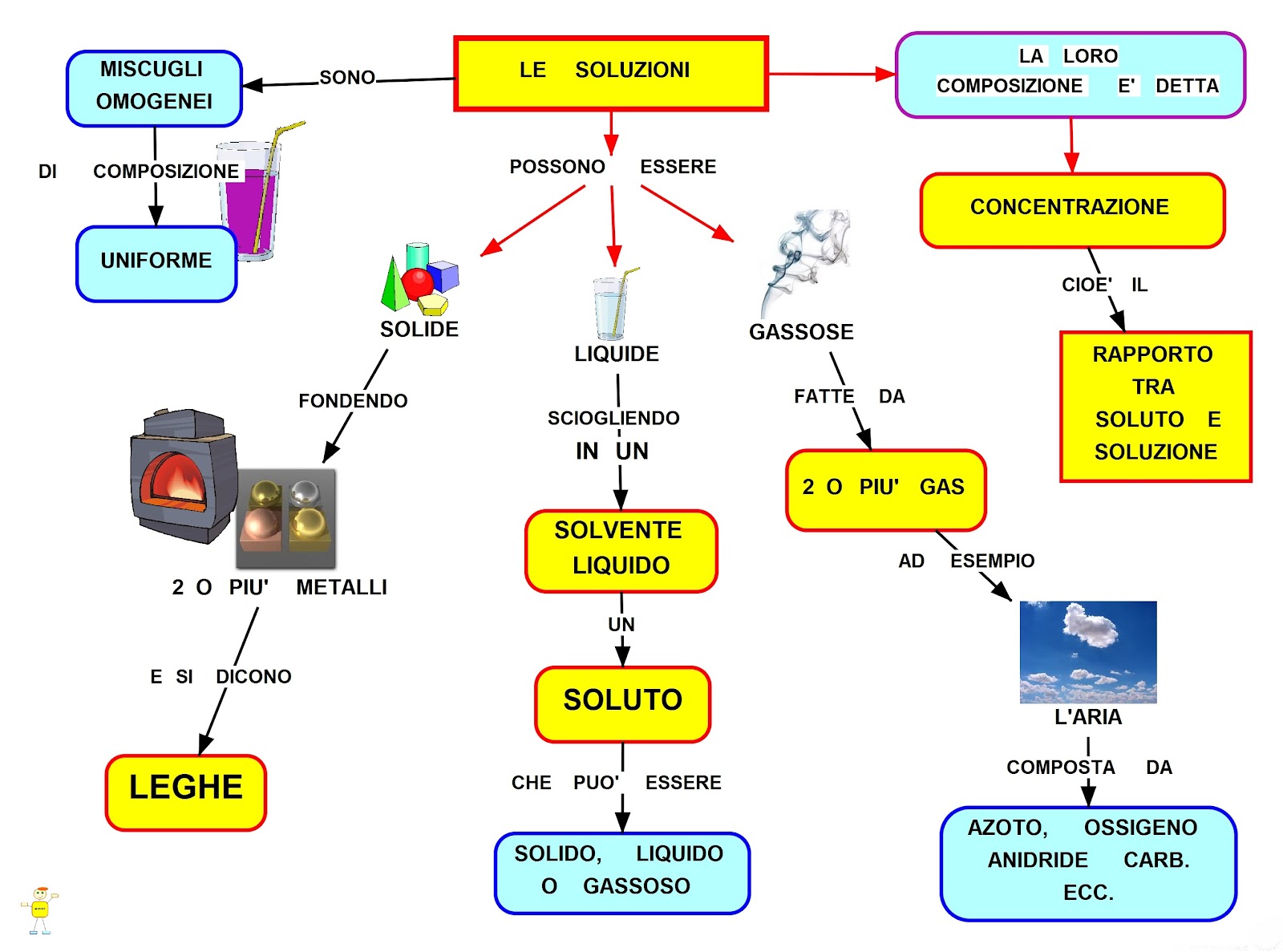
Mappa Concettuale pubblicata per gentile concessione di Mapper (http://mapper-mapper.blogspot.it/).